呀
| 维生素C及其制剂的含量测定 | ||||||||||||||||||
| 【来源:桂西制药】【作者:admin】【发布时间:2010-12-16】 |
||||||||||||||||||
|
一、实验目的
1.1掌握直接碘量法的测定原理及操作方法。
1.2掌握常用辅料对制剂含量测定的干扰及排除。
1.3掌握含量计算方法。
二、实验原理
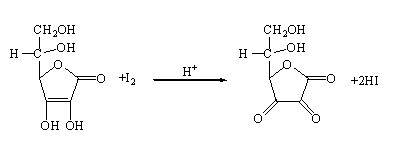
维生素C具有强还原性,在醋酸酸性条件下,可被碘定量氧化。根据消耗碘滴定液的体积,即可计算维生素C的含量。片剂测定时,应过滤除去赋形剂的干扰。注射剂测定时要加丙酮2ml,以消除抗氧剂的干扰。
 三、实验试剂
三、实验方法
维生素C注射液
本品为维生素C的灭菌水溶液,为无色至微黄色的澄明液体。可加适量的焦亚硫酸钠为稳定剂。含维生素C应为标示量的90.0%~110.0%。精密量取本品适量(约相当于维生素C0.2g),加水15ml与丙酮2ml,摇匀,放置5min,加稀醋酸4ml与淀粉指示液1ml,用碘滴定液(0.05mol/L)滴定,至溶液显蓝色并在30s内不褪。每1ml碘滴定液(0.05mol/L)相当于8.806mg的C6H8O6。
计算方法:
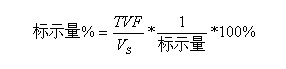 式中:VS为样品取样量; V为实验消耗滴定液的体积; T为碘滴定液的滴定度;F为校正因子。
四、实验记录与结果
1、滴定液标定
2、维生素C的测定
其中VS为样品取样量; V为实验消耗滴定液的体积; T为碘滴定液的滴定度;F为校正因子。
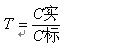 四、注意事项
维生素C易被空气中的O2氧化,因此过滤、滴定等操作应快。接近终点时则应减慢滴定速度,滴定至溶液显蓝色并持续30s不褪确认为终点。
| ||||||||||||||||||
| 【返回顶部】【关闭】【打印】 |